Санитарно-гигиенические нормативы по микробиологическим показателям пищевых продуктов включают контроль четырех групп микроорганизмов:
- санитарно-показателъные микроорганизмы:
- КМАФАнМ – количество мезофильных аэробных и факультативно-анаэробных микроорганизмов; БГКП (колиформные бактерии) – бактерии группы кишечной палочки; энтерококки; кишечные бактериофаги (колифаги);
- условно-патогенные микроорганизмы:
- Escherichia coli; Staphylococcus aureus; Bacillus cereus;
- сульфитредуцирующие бактерии (Clostridium perfringens); бактерии рода Proteus; Vibrio parahaemolyticus;
- патогенные микроорганизмы: сальмонеллы; Listeria monocytogenes;
- микроорганизмы порчи: дрожжи, плесневые грибы, молочнокислые бактерии, гнилостные бактерии;
- микроорганизмы заквасочной микрофлоры молочнокислых продуктов и пробиотические микроорганизмы в продуктах с нормируемым уровнем биотехнологической микрофлоры и в пробиотических продуктах.
12.1. ОБЩАЯ ХАРАКТЕРИСТИКА САНИТАРНО-ПОКАЗАТЕЛЬНЫХ МИКРООРГАНИЗМОВ
Нарушение санитарно-гигиенических правил изготовления, транспортировки, хранения продуктов питания может привести к их контаминации патогенными и условно-патогенными микроорганизмами, что способствует возникновению пищевых инфекций и отравлений.
Патогенные микроорганизмы попадают на пищевые продукты, в воду, почву, воздух из выделений больных людей и животных, а также из выделений бактерио- и вирусоносителей. Индикация патогенных бактерий из объектов внешней среды вызывает ряд трудностей, так как они присутствуют в объектах среды в низких концентрациях и их наличие не удается зафиксировать в межэпидемические периоды. Для их обнаружения и культивирования требуются довольно сложные питательные среды, а работу с патогенными микроорганизмами должны осуществлять специально подготовленные специалисты.
Показателями санитарного неблагополучия объектов внешней среды избраны в том числе микроорганизмы, постоянно обитающие в организме человека и теплокровных животных (толстом отделе кишечника и верхнем отделе дыхательных путей). Они являются комменсалами и проявляют условно-патогенные свойства лишь при изменении условий. Эти микроорганизмы и были названы санитарно-показательными.
Санитарно-показательные микроорганизмы должны отвечать следующим требованиям:
- постоянно содержаться в выделениях человека и теплокровных животных во внешнюю среду в больших количествах;
- после выделения сохранять жизнеспособность в течение времени, близкого к срокам выживаемости патогенных микробов;
- не размножаться в окружающей среде и не изменять свои биологические свойства;
- не зависеть от присутствия других микроорганизмов, которые способны подавлять или стимулировать их рост;
- быть достаточно типичными, чтобы их дифференциальная диагностика не вызывала затруднений.
Причем методы идентификации СПМО должны быть простыми, доступными и экономичными.
БГКП. Понятие БГКП утилитарное (санитарно-бактериологическое и экологическое), но не таксономическое. Группа БГКП представлена микроорганизмами родов Esherichia, Citrobacter, Enterobacter, Serratia, Klebsiella, экологические особенности которых определяют их индикаторную значимость. Это грамотрицательные, не образующие спор, короткие палочки, сбраживающие глюкозу и лактозу с образованием кислоты и газа при 37,0 ± 0,5°С в течение 24–48 ч, не обладающие оксидазной активностью.
ОКБ (общие колиформные бактерии) – это грамотрицательные оксидазонегативные палочки, которые на среде Эндо расщепляют лактозу при 37°С в течение 48 ч.
Род Escherichia включает типовой вид Е. coli и служит показателем свежего фекального загрязнения. Для идентификации Е. coli используют биохимические тесты, учитывая способность к ферментации лактозы при 44,0 ± 0,5°С и отсутствие роста на цитратсодержащих средах. Обнаруженных в воде представителей рода Escherichia относят к термотолерантным колиформным бактериям, в лечебных грязях – к фекальным колиформным бактериям, в пищевых продуктах – к Е. coli.
Кишечная палочка не является идеальным санитарно-показательным микроорганизмом.
Недостатки кишечной палочки как СПМО: обилие аналогов во внешней среде; изменчивость во внешней среде; недостаточная устойчивость к неблагоприятным воздействиям; недостаточно длительное выживание в продуктах по сравнению с шигеллами Зонне, сальмонеллами, энтеровирусами; способность к размножению в воде; нечеткий индикатор в отношении присутствия сальмонелл.
Бактерии рода Citrobacter доказательно обнаружены при эпидемических вспышках, протекающих по типу диспепсий, гастроэнте-роколитов, пищевых токсикоинфекций.
Энтерококки (Enterococcus faecalis и Enterococcus faecium) имеют следующие преимущества. Преимущества энтерококка как СПМО: постоянно находится в кишечнике человека и животных; постоянно выделяется во внешнюю среду; Е. faecalis в основном обитает в кишечнике человека; Е. faecium обнаруживается в кишечнике животных, хотя сравнительно редко также отмечается и Е. faecalis faecalis; не способен размножаться во внешней среде; не изменяет своих свойств во внешней среде; не имеет аналогов во внешней среде; устойчив к неблагоприятным воздействиям внешней среды.
К хлору энтерококк в четыре раза устойчивее по сравнению с кишечной палочкой. Благодаря этому признаку энтерококк используют при проверке качества хлорирования воды, а также как индикатор качества дезинфекции. Он выдерживает температуру 60°С, что позволяет применять его как показатель качества пастеризации. Может быть использован в качестве индикатора при исследовании соленых продуктов, морской воды, так как по сравнению с кишечной палочкой устойчив к растворам, имеющим концентрацию поваренной соли 6,5–17%, в которых кишечная палочка гибнет или становится атипичной. Устойчив к рН в диапазоне 3–12, что делает его индикатором фекального загрязнения при исследовании кислых продуктов. Для индикации энтерококков разработаны высокоселективные среды.
Показателем свежего фекального загрязнения воды в настоящее время узаконена энтерококкометрия. При обнаружении в воде атипичных кишечных палочек присутствие энтерококков становится главным показателем свежего фекального загрязнения. В настоящее время узаконена энтерококкометрия молока, котлет в целях выяснения эффективности их термической обработки.
Протей. Бактерии рода Proteus встречаются в 98% случаев в выделениях из кишечника человека и животных, из них в 82% случаев – это P. mirabilis. На загрязнение объектов разлагающимися субстратами указывает обнаружение протея в воде и продуктах, что свидетельствует о крайнем санитарном неблагополучии. При обнаружении протея в пищевых продуктах их бракуют, а воду не разрешают употреблять для питья.
Clostridium perfringens. У С. petfringens как СПМО есть свои достоинства и недостатки:
- не постоянно обнаруживается в кишечнике человека;
- длительно сохраняется во внешней среде за счет спорообразования, поэтому не свидетельствует о свежем фекальном загрязнении;
- погибает от действия сопутствующей микрофлоры;
- имеет споры, устойчивые к концентрациям активного хлора 1,2–1,7 мг/л воды;
- может служить косвенным показателем наличия в воде энтеровирусов.
Для прорастания спор клостридий необходим температурный шок (прогревание при 75°С в течение 15–20 мин). Определение титра С. perfringens рекомендовано при текущем санитарном надзоре за состоянием территории. Тесты на обнаружение сульфитредуцирующих клостридий в воде предусматривают стандарты России, Румынии, США. Определение С. perfringens проводят в воде открытых водоемов, почве, лечебных грязях, мясных продуктах.
Термофилы. Эта группа СПМО, в основном спорообразующих видов, растет при температуре 55–60°С. Обитают они во внешней среде и являются показателем загрязнения навозом и компостом. Под действием термофилов при гниении навоза или компоста температура поднимается более 60°С, и термофилы бурно размножаются. Их определяют при исследовании почвы, а также в консервах, используя как индикатор термической обработки.
Бактериофаги кишечной палочки, фаги сальмонелл и шигелл используют в качестве СПМО. Они обнаруживаются там, где есть соответствующие бактерии, к которым эти фаги специфичны. Во внешней среде фаги выживают более 9 мес. Они ценны как показатель фекального загрязнения, особенно энтеровирусами, так как фаги выделяются из сточных вод с той же частотой, что и энтеровирусы.
Сальмонеллы. Сальмонеллы относятся к наиболее распространенным микроорганизмам, вызывающим острые кишечные заболевания (ОКЗ). Они могут служить индикатором других ОКЗ с аналогичными патогенезом и эпидемиологией. Поступают во внешнюю среду только с фекалиями человека и животных. Размножаются в почве при наличии в ней большого количества органических веществ, однако могут размножаться даже в чистой воде. При определении сальмонелл в воде следует вычислять не только процент положительных обнаружений, но и НВЧ. По этому показателю можно оценить эпидемиологическую ситуацию.
Синегнойная палочка. Способна размножаться во внешней среде. Обнаруживается в фекалиях здоровых людей в 11%, а у животных – в 7% (т.е. непостоянно). Методы индикации просты, но только в отношении пигментных форм, а во внешней среде преобладают безпигментные формы, которые распознавать трудно. Обнаруживается в 90% случаях в сточных водах, в больничных палатах. Наличие синегнойной палочки свидетельствует о неблагополучном санитарном состоянии лечебного учреждения. Роль ее выросла в связи с распространением антибиотикоустойчивых штаммов и появлением большого количества носителей на коже и в моче.
Грибы рода Candida постоянно присутствуют в организме человека: в фекалиях в 10–90% случаев, в слизи верхних дыхательных путей – в 15–50%, на коже – в 1–100%. Они обнаруживаются везде, где есть сахаросодержащие вещества. Первоисточниками в природе являются человек и животные. Они очень устойчивы к неблагоприятным воздействиям внешней среды, причем даже более, чем патогенные бактерии. Их можно использовать в качестве индикаторов эффективности дезобработки.
К СПМО относится a-зеленящий стрептококк (S. salivarius). У него есть двойники, такие как S. lactis, bovis, equinus, cremoris. Но эти двойники редко обнаруживаются в жилых помещениях. Зеленящими могут быть и энтерококки, но они сами являются СПМО. Другим санитарно-показательным стрептококком является b-гемолитический стрептококк, он обнаруживается в 80% у людей, в основном страдающих воспалительными заболеваниями верхних дыхательных путей. Он обладает гемолитическими свойствами. Показателем санитарного неблагополучия является и золотистый стафилококк. Именно этот вид стафилококка связан с присутствием людей и некоторых животных. В среднем у здоровых людей золотистый стафилококк обнаруживается в 30% случаев, а у медицинского персонала – до 96%. Этот вид стафилококка отличается длительностью выживания и устойчивостью во внешней среде. Он может быть косвенным индикатором загрязнения воздуха вирусами. Использование золотистого стафилококка, как наиболее информативного СПМО, рекомендовано при исследовании воздуха жилых помещений, жилых отсеков космических кораблей, подводных лодок, лечебно-профилактических учреждений.
На роль СПМО выдвигаются также антибиотикорезистентные стафилококки и микрококки. Причем 5–6-кратное превышение указанных СПМО в воздухе больничных помещений по сравнению с воздухом небольничных помещений следует оценивать как плохой прогностический признак.
Бделловибрионы предложены в качестве СПМО. Это аэробные грамотрицательные палочки, подвижные, имеют жгутики. Размеры 0,25 × 1,2 мкм. Являются хищниками по отношению к другим бактериям, поражают только грамотрицательные палочки. На одном из полюсов бделловибрионов есть полость, где скапливается экзотоксин и липолитии ческий фермент, который и растворяет клеточную стенку бактерий. Отличают их друг от друга по литической активности: одни лизируют только псевдомонады, другие – только аэромонады. Бделловибрионы применяют для биологической очистки воды (искусственно выпускают в воду плавательных бассейнов), используют как СПМО по загрязнению воды. В местах сброса сточных вод количество бделловибрионов достигает 3,0 · 103 КОЕ/см3, а дальше от сброса – 10 КОЕ/см3. Выделяют бделловибрионы по методу Грация, но для постановки пробы необходимо иметь индикаторный штамм Е. coli. К-12. Количество их выражают в бляшкообразующих единицах (БОЕ/см3).
Аэромонады. Они в больших количествах содержатся в сточных водах и обладают большой энергией размножения. Служат показателем нагрузки сточных вод на водоем и имеют такое же значение, как ОМЧ. При большой концентрации аэромонад в воде может наступить пищевое отравление.
12.2. САНИТАРНО-ПОКАЗАТЕЛЬНЫЕ ГРУППЫ МИКРООРГАНИЗМОВ.
12.2.1. Количество мезофильных аэробных и факультативно анаэробных микроорганизмов (КМАФАнМ)
Количество микроорганизмов, обнаруженных в единице массы или объема сырья, вспомогательных материалов или готовой продукции, характеризуют показателем КМАФАнМ. Это наиболее распространенный микробиологический тест, используемый для контроля качества пищевой продукции, за исключением тех продуктов, в технологии которых используется специфическая микрофлора (ферментированные молочные продукты, квашеные овощи, квас и др.). Показатель КМАФАнМ дает представление о присутствии в продукте микроорганизмов различных таксономических групп и отражает нарушения, допущенные в технологии пищевого продукта. Превышение допустимых норм КМАФАнМ свидетельствует о недостаточной тепловой обработке продукта, нарушении санитарно-гигиенического режима его производства, правил транспортировки и хранения. Показатель КМАФАнМ характеризует качество пищевого продукта и его безопасность для потребителя (табл. 12.1).
Таблица 12.1
Показатель КМАФАнМ в пищевых продуктах
(Галынкин и др., 2007)

Метод оценки качества продуктов по показателю КМАФАнМ имеет ряд недостатков: используемый чашечный метод дает заниженные результаты по количеству микроорганизмов, так как колонии на плотной среде могут образовываться не из одной клетки, а из их значительного скопления; не учитываются группы термофильных и психрофильных микроорганизмов, поскольку инкубация чашек проводится при одном температурном режиме – 37°С; не учитываются анаэробные микроорганизмы, не растущие в чашках при доступе кислорода воздуха; тест не может быть использован для большой группы пищевых продуктов, содержащих специфическую микрофлору (кисломолочных, пробиотических, квашеных); тест не дает представления о качественном составе микроорганизмов, присутствующих в продукте, в том числе патогенных.
12.2.2. Бактерии группы кишечной палочки (БГКП – колиформные бактерии)
Выявление БГКП в пищевых продуктах свидетельствует об их фекальном загрязнении. БГКП могут попадать в продукты из воды, с оборудования, рук рабочего персонала и из других источников. БГКП подразделяют на две подгруппы:
- общие колиформные бактерии, расщепляющие глюкозу, лактозу и маннит с образованием кислоты и газа при 37°С в течение 24 ч;
- термотолерантные колиформные бактерии, расщепляющие глюкозу и лактозу с образованием кислоты и газа при 43–44,5°С.
В группу БГКП входят роды Escherichia, Enterobacter, Citrobacter, Klebsiella, Serratia (табл. 12.2).
Род Escherichia. Типовым видом этого рода является Escherichia coli. Он играет важную роль в микробиоценозе кишечника человека и животных.
Е. coli – мелкие грамотрицательные палочки с закругленными концами размером
(2–3) × (0,5–0,7) мкм. Не образуют спор, неподвижны. Есть варианты подвижные за счет перитрихиально расположенных жгутиков, капсул не имеют. Факультативные анаэробы. Получают энергию как в процессе дыхания, так и при брожении. При сбраживании углеводов Е. coli накапливают кислоты – молочную, уксусную, янтарную (положительная реакция с метиловым красным) и газы – СO2 и Н2 (бродильная проба). Эшерихии хорошо растут на простых питательных средах. Оптимальная температура роста составляет 37°С, оптимальное значение pH среды — 7,0–7,4.
Таблица 12.2
Признаки родов, относящихся к БГКП
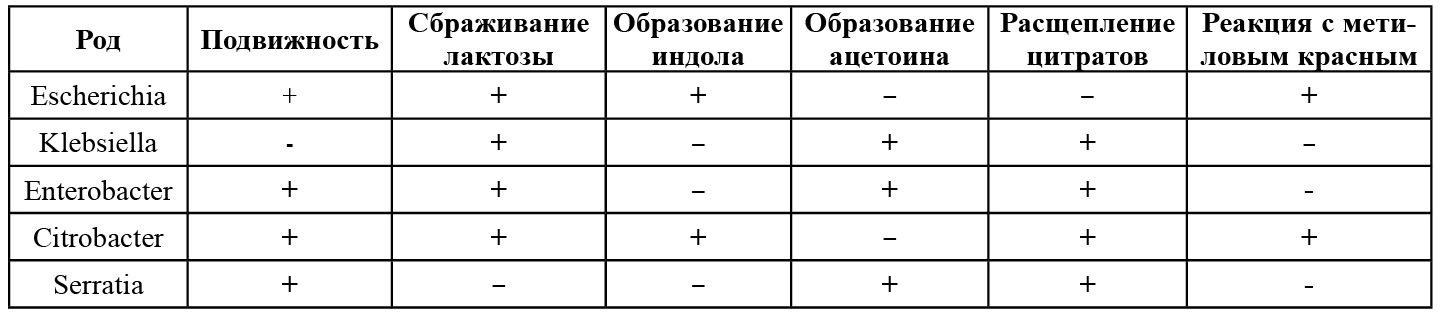
Род Enterobacter. Представители рода обнаруживаются в пресной воде, почве, сточных водах, на растениях, овощах; их выделяют из кишечника человека и животных. Виды рода в последние годы выделяют при острых желудочно-кишечных заболеваниях, диспепсии, инфекциях желчных и мочевых путей, гнойных поражениях мозговых оболочек, сепсисе у людей и животных. Типовой вид – Е. cloacae.
Клетки Enterobacter – прямые палочки размером (2–3) × (0,5– 0,6) мкм, перитрихи, грамотрицательные, не образуют спор и капсул. Оптимальная температура роста 30–37°С. Биохимические признаки видов этого рода: образование ацетоина при сбраживании углеводов (положительная реакция Фогес–Проскауэра), расщепление цитрата натрия в среде Симмонса.
Род Citrobacter (citrus – (лимон) и bacter). Представители этого рода присутствуют в фекалиях человека и животных, почве, сточных водах, пищевых продуктах. При определенных условиях они могут вызывать заболевания, протекающие по типу гастроэнтеритов, диспепсий. При развитии гнойно-воспалительных процессов наиболее значимым является вид C. freundii, который является типовым видом данного рода. Клетки цитробактеров – прямые палочки размером (1–6) × (0,5–0,8) мкм, одиночные или в парах. Перитрихи. Спор и цист не образуют, капсул не образуют. С. freundii продуцирует сероводород. На кровяном агаре вокруг колоний образуются четкие зоны гемолиза.
Род Klebsiella назван в честь бактериолога Э. Клебса. Бактерии этого рода выделяют из воды, почвы, пищевых продуктов. Они присутствуют в биоценозах носоглотки, кишечника. Вызывают заболевание клебсиеллез у детей в возрасте до 1 года. Заболевание протекает в виде диареи, менингита, бронхопневмонии, гнойно-септических воспалений. Представители рода: К. pneumonia, К mobilis и сапрофитные виды: К. planticola, К. terrigena. Это прямые палочки размером (0,6–6,0) × (0,3–1,0) мкм, одиночные или в парах. Отличаются от других энтеробактерий характерными признаками: обладают классической полисахаридной капсулой и лишены жгутиков. Типовой вид – Klebsiella pneumonia.
Род Serratia. Название рода связано с именем итальянского физика Серафино Серрати. Они встречаются в почве, воде, на поверхности растений, а также в пищеварительном тракте человека, насекомых и грызунов в качестве комменсалов. У лиц с ослабленной иммунной системой серрации могут вызвать гнойные воспаления самой различной локализации. Типовой вид – Serratia marcescens. Serratia marcescens – это прямые мелкие палочки размером (0,5–0,8) × (0,9–2,0) мкм. Перитрихи при определенных условиях способны образовывать капсулу. Большинство колоний Serratia окрашены в различные оттенки красного цвета за счет образования пигмента продигиозина.
При характеристике БГКП учитываются следующие дифференциально-диагностические признаки:
- инкубация посевов при едином температурном режиме – 37°С;
- способность ферментировать лактозу – характер роста на среде Эндо (так называемый лактозный тест). Учитываются колонии темно-красные, с металлическим блеском или без него;
- оксидазный тест: колонии на среде Эндо исследуются на наличие оксидазы. Для дальнейшей идентификации оставляют оксидазоотрицательные колонии. Колонии с положительным оксидазным тестом, относящиеся к грамотрицательным бактериям родов Pseudomonas, Aeromonas, Vibrio, не учитываются;
- препараты из характерных колоний окрашивают по Граму – учитываются грамотрицательные палочки;
- бродильная проба на среде Гисса с глюкозой для обнаружения способности бактерий ферментировать глюкозу с образованием кислоты и газа.
Помимо БГКП возбудителями кишечных заболеваний, вызванных употреблением контаминированных пищевых продуктов, могут быть также бактерии родов Morganella и Providencia из семейства Enteribacteriaceae.
Обнаружение энтерококков в пищевых продуктах свидетельствует о их свежем фекальном загрязнении или о нарушениях технологических параметров производства. Они выделяются в среду с фекалиями в значительных количествах: в 1 г фекалий до
108–109 жизнеспособных клеток, что на порядок меньше, чем кишечных палочек. Энтерококки – сферические или овальные кокки, расположенные попарно или короткими цепочками, грамположительные, неподвижные, не образуют эндоспор и капсул. Факультативные анаэробы. Сбраживают различные углеводы с образованием в основном молочной кислоты, снижая рН среды до 4,2–4,6. Оптимальная температура – 37°С, диапазон роста — 10–45°С. К энтерококкам относят Enterococcus faecalis, Е. faecium, Е. durans. Типовой вид – Enterococcus faecalis. Особенностью энтерококков является их высокая устойчивость к неблагоприятным факторам внешней среды. Они выдерживают нагревание при 65°С в течение 30 мин, устойчивы к высоким концентрациям хлорида натрия (6,5–17%) и желчи (до 40%), остаются жизнеспособными в диапазоне pH 3–12. Эти особенности позволяют дифференцировать роды Enterococcus от Streptococcus и Lactococcus.
Бактериофаги постоянно содержатся в кишечнике млекопитающих, в объектах внешней среды, загрязненных фекалиями и навозом. Поэтому бактериофаги являются показателями фекального загрязнения воды, почвы энтеробактериями, в том числе патогенными. Они значительно дольше сохраняются во внешней среде по сравнению с энтеробактериями. Поэтому колифаги могут быть обнаружены как при свежем фекальном загрязнении объекта, опасном в эпидемиологическом отношении, так и после отмирания всех патогенных энтеробактерий. Санитарно-показательное значение колифагов достойно оценено после вспышек вирусных заболеваний (полиомиелита, инфекционного гепатита и др.), передаваемых через воду. Многие энтеровирусы и аденовирусы, являющиеся возбудителями указанных заболеваний, более стойки во внешней среде, чем кишечная, брюшно-тифозная и дизентерийная палочки. Отсюда следует, что ряд вирусов может сохранять свою жизнеспособность даже в условиях, неблагоприятных для патогенных и сапрофитных энтеробактерий, и представлять определенную опасность для человека. Таким образом, обнаружение колифагов используют в качестве дополнительного теста, свидетельствующего о фекальном загрязнении исследуемого объекта и возможном присутствии возбудителей вирусных инфекций.
12.3. УСЛОВНО-ПАТОГЕННЫЕ МИКРООРГАНИЗМЫ
Внутри этого вида имеются энтеропатогенные варианты, вызывающие у млекопитающих различные заболевания: колиты, энтероколиты, эшерихиозы и др. Род Escherichia включает в себя еще шесть видов, в том числе Е. coli, Е. albertii, Е. blattae, Е. fergusonii, Е. vulneris, Е. hermannii. Этим свойством обладает также Enterobacter sakazakii. В связи с тем, что эти виды не ферментируют лактозы, они не включены в группу колиформов. Е. vulneris выделен из ран человека, а Е. hermannii – из анализов больных.
Е. coli является типичным представителем рода Escherichia, и соответственно более точным индикатором фекального загрязнения, чем остальные виды. Всегда желательно определить ее количество в популяции. Классическим методом подобного определения является «Формула IMViC», где I – продукция индола; М – реакция на метиловый красный; Vi – реакция Вогса–Проскера на продукцию ацетона; С – использование цитрата. Согласно указанной формуле для колиформных бактерий Е. coli и Е. aerogenes характерны следующие результаты.
Е. coli продуцирует индол (I), дает реакцию на метиловый красный (М), а показатели Vi и С для Е. coli не характерны. В то же время Е. aerogenes по указанным показателям формулы дает противоположный эффект.
Штаммы кишечных палочек при ослабленном иммунитете могут вызывать гнойно-воспалительные заболевания за пределами пищеварительного тракта: менингит, цистит, холецистит, отит, мастит, коли-сепсис, пневмонию, бронхиальную астму, конъюнктивит. У детей до двух лет энтеропатогенная кишечная палочка вызывает тяжелую диарею, смертность от которой во всем мире составляет около 24%. В связи с этим в продуктах питания для детей не допускается присутствие Е. coli в определенной массе или объеме продукта (СанПин 2.3.2.1078–01, Федеральный закон от 12 июня 2008 г. № 88-ФЗ «Технический регламент на молоко и молочную продукцию»).
В конце 1980-х гг. были зафиксированы необычные желудочно-кишечные заболевания, характеризующиеся острой спазматической болью, небольшим повышением температуры, серьезной диареей с выделением большого количества крови, иногда заканчивающиеся летальным исходом. В разных странах вспышки заболевания возникали при употреблении гамбургеров с недожаренной говядиной, рубленых бифштексов, вяленой оленины (США); пирогов с мясом, козьего сыра (Шотландия); полусухой ферментированной колбасы (Южная Австралия); побегов редьки дайкон (Япония) или контаминированной питьевой воды (Канада). Возбудителем заболевания явился штамм Escherichia coli 0157:Н, обладающий геном, ответственным за продуцирование веротоксина. Этот токсин известен также как шигатоксин из-за своего сходства с токсином, продуцируемым бактериями рода Shigella – возбудителями дизентерии. Главными факторами патогенности штамма Е. coli 0157:Н являются способность прикрепляться к стенке кишечника человека и продуцировать сильнодействующие веротоксины. Как показали исследования, носителями и распространителями штамма Е. coli 0157:Н признаны овцы, крупный рогатый скот, свиньи.
В настоящее время эшерихии принято подразделять на несколько категорий.
- Энтеропатогенные кишечные палочки (ЭПКП, ЕРЕС). Они вызывают заболевания, сходные по симптомам с сальмонеллезом.
- Энтеротоксигенные кишечные палочки (ЭТКП, ЕТЕС). Они способны продуцировать энтеротоксины. Обусловливают холероподобный эшерихиоз. Среди ЕТЕС различают штаммы, продуцирующие термолабильный (ТЛ) энтеротоксин, иммунологически близкий энтеротоксину холерных вибрионов; штаммы, вырабатывающие термостабильный (ТС) энтеротоксин, и штаммы, образующие оба (ТЛ, ТС) энтеротоксина. Энтеротоксигенные эшерихии вызывают до 5% всех диарейных заболеваний.
- Энтероинвазивные кишечные палочки (ЭИКП, ЕIЕС), обладающие способностью инвазировать эпителий кишечника и вызывать заболевания, подобные шигеллезу (дизентериеподобный эшерихиоз). Имеют много общих 0-антигенов с шигеллами. Экология энтероинвазивных эшерихий изучена слабо.
- Энтерогеморрагические кишечные палочки (ЭГКП, ЕНЕС), являющиеся наиболее этиологически значимыми в эпидемиологическом плане. Образуют шигаподобный токсин 1 (веротоксин 1) и шигаподобный токсин 2 (веротоксин 2), действием которых во многом обусловлена симптоматика кишечных инфекций, обусловленных энтерогеморрагическими кишечными палочками. Вызывают достаточно характерную симптоматику: геморрагический колит, сопровождающийся кровянистой диареей с присутствием в испражнениях значительной примеси лейкоцитов, схваткообразные боли в абдоминальной области, развитие гемолитико-уремического синдрома. Смертность может достигать 10%. Основным естественным резервуаром ЕНЕС является крупный и мелкий рогатый скот, также носителями энтерогеморрагических кишечных палочек могут быть такие домашние животные, как свиньи, лошади, олени, птицы, собаки и кошки. Из продуктов питания важнейшее значение как источник инфекции имеют мясные продукты, а также молоко. При проведении мониторинга ЕНЕС среди сельскохозяйственных животных в Европе было обнаружено, что в Германии около 20% животных и 2,6% исследованных проб мяса крупного рогатого скота были заражены Е.соli O157:Н7. При проведении мониторинга ЕНЕС серовара O157:Н7 в хозяйствах Рязанской, Воронежской, Тульской и Орловской областей обнаружено, что бактерионосительство среди крупного рогатого скота составило 2,6%, среди свиней – 0,9% и птиц – 0,8% (2006 г.).
- Энтероадгезивные (энтероагрегирующие или энтероагрегативные) кишечные палочки (ЭАКП) не инвазивны, не образуют цитотоксины и не имеют плазмидного фактора адгезии. ЭАКП пока не представлены какими-либо серогруппами. Энтероагрегативные кишечные палочки выделены в отдельную группу. Эшерихии данной группы обладают способностью вызывать заболевания главным образом у особей с ослабленной сопротивляемостью инфекции.
- Диффузно-агрегирующие кишечные палочки (ДАКП). Факторами их вирулентности является плазмидоопосредованное агрегативное прикрепление, предупреждающее абсорбцию жидкости.
Для установления наличия и подсчета Е. coli и колиформных бактерий разработаны методы: 1) СПК – стандартный подсчет колоний или аэробный подсчет колоний (АПК), используемый для подсчета живых клеток или колониеобразующих единиц (КОЕ); 2) НВЧ – наиболее вероятное число, т.е. статистическое определение количества жизнеспособных клеток; 3) редуктазная проба для оценки числа жизнеспособных клеток, обладающих окислительно-восстановительной способностью; 4) ОМС – прямой микроскопический подсчет, с помощью которого определяют количество жизнеспособных и нежизнеспособных клеток.
Стафилококки относят к представителям нормофлоры млекопитающих. Местом их локализации являются слизистые оболочки верхних дыхательных путей и кожные покровы. В небольшом количестве они присутствуют в кишечнике здоровых особей. Во внешнюю среду стафилококки попадают при кашле, чихании, разговоре, а также из гнойничковых ран на коже, из мест воспалений.
Стафилококки представлены тремя видами: золотистым – S. aureus – патогенным; эпидермальным – S. epidermidis – условно-патогенным и сапрофитным – S. saprophiticus – непатогенным. Стафилококки имеют диаметр 0,6–1,2 мкм. Они неподвижны, грамположительны, спор и капсул не образуют. На мясопептонном агаре стафилококки образуют довольно крупные выпуклые колонии диаметром от 1 до 4 мм, с ровными краями, гладкие, блестящие, реже – шероховатые. При температуре 20–25°С, доступе кислорода и рассеянном свете стафилококки вырабатывают пигмент золотистого (S. aureus), лимонно-желтого (S. saprophiticus) или белого (S. epidermidis) цвета. Стафилококки являются аэробными или факультативно-анаэробными микроорганизмами, размножаются на обычных питательных средах с pH 7,2–7,4; оптимальная температура роста — 25–37°С. Устойчивы к температуре 80°С в течение 20–30 мин. Их рост задерживается хлоридом натрия
(> 12 %), сахаром (> 60 %) и активной кислотностью среды (pH < 4,5).
- aureus обладает высокой степенью толерантности к таким веществам, как теллурит, хлорид ртути, неомицин, полимиксин и азид натрия, которые обычно используются в качестве селективных агентов, добавляемых в культуральные среды. Бактерии этого вида можно отличать от других видов стафилококков по их большей устойчивости к акрифлавину. S. aureus чувствительны к солям борной кислоты.
Что касается pH, то S. aureus может расти при pH от 4,0 до 9,8, но оптимальные значения находятся в интервале 6–7.
Что касается активности воды, то S. aureus является уникальным по своей способности расти при значении этого параметра более низком, чем все другие негалофильные бактерии. Рост S. aureus был продемонстрирован даже при значении aw = 0,83 при всех других идеальных условиях, несмотря на то что значение aw = 0,86 обычно считается минимальным.
Люди, страдающие носовой инфекцией или имеющие нарывы на руках стафилококкового происхождения, являются потенциальным источником заражения пищевых продуктов.
Вместе с тем велика вероятность заражения инфекцией, вызываемой S. aureus, при употреблении сырого молока от больных стафилококковым маститом коров или использовании молока от таких коров для приготовления сыра и сырной продукции.
В качестве санитарно-показательных бактерий для воздуха закрытых помещений предложены гемолитические стрептококки и золотистые стафилококки. Появление в воздухе грамотрицательных бактерий – показатель его возможного антисанитарного состояния.
В качестве тест-объекта для контроля качества дезинфекции используют S. aureus.
Bacillus cereus (восковидная палочка) широко распространена в почве, в воде открытых водоемов. Bacillus cereus – крупная грамположительная палочка размером 8 × (0,9–1,5) мкм, подвижная, образует эндоспоры, может формировать капсулу. Микроаэрофил. Температура роста — 30–32°С; колонии на мясопептонном агаре бывают крупными, плоскими, с изрезанными краями, иногда пигментированными. На кровяном агаре вокруг колоний наблюдаются резко очерченные зоны гемолиза. Bacillus cereus устойчива к высушиванию, высоким концентрациям хлорида натрия (до 10–15 %), сахара (до 30–60%), споры выдерживают нагревание до 105–125°С в течение 10 мин. Чувствительна она к уксусной кислоте.
12.3.4. Сульфитредуцирующие бактерии
(Clostridium perfringens)
Постоянным обитателем кишечника млекопитающих является С. perfringens. Это палочка размером (5–8) × (1–2) мкм, грамположительная, подвижная, образующая эндоспоры. В организме млекопитающих Clostridium perfringens способна образовывать капсулы. Колонии имеют вид дисков или плотных комочков ваты. На поверхности кровяного агара Clostridium perfringens образует влажные, серовато-зеленые колонии с четкой зоной гемолиза.
Обладает свойством восстанавливать сульфиты (сульфитредуцирующая) и обнаруживается на среде Вильсона–Блера в виде черных колоний за счет превращения хлорида железа в сульфат железа. Возбудитель ферментирует множество сахаров с образованием газа. Рост микроорганизма в молоке сопровождается образованием губчатого сгустка, «подбрасываемого» к ватной пробке пробирки за счет газообразования. С. perfringens – анаэроб, но может расти в присутствии небольшого количества кислорода. Температура роста — 37–39°С. В пищевых продуктах размножается при температуре не ниже 15–20°С. Размножение Clostridium perfringens подавляется при значении pH среды ниже 3,5–4,0 и концентрации NaCl 10–12%. На вегетативные клетки наиболее активно действуют пероксид водорода, раствор фенола в обычных концентрациях, многие антибиотики, эффективные для грамположительных бактерий. Споры С. perfringens выдерживают кипячение в течение 15–90 мин. Преимуществом С. perfringens перед кишечными палочками как санитарно-показательными микроорганизмами является их быстрая и несложная индикация на среде Вильсона–Блера. Тест на присутствие С. perfringens может быть использован как показатель загрязнения пищевых продуктов другими патогенными кло-стридиями – возбудителями ботулизма или столбняка.
Обнаружение С. perfringens в окружающей среде является показателем давнего фекального загрязнения. Если их количество велико и они обнаруживаются вместе с БГКП, то это свидетельствует о свежем фекальном загрязнении. На присутствие С. perfringens необходимо проверять воду, используемую на предприятиях консервной промышленности, поскольку нахождение клостридий в консервах особенно опасно. Они не должны обнаруживаться в 100 см3 исследуемой воды.
Индикацию чаще всего проводят с помощью метода Шукевича посевом 0,1 см3 из разведений исследуемого продукта (от 10-1 до 10-6) в конденсационную влагу свежескошенного агара в пробирке. После 18–24 ч инкубации при 37°С на поверхности агара наблюдается характерный вуалевидный сплошной рост протея.
Род Proteus входит в семейство кишечных бактерий – Enterobacteriaceae. В пищевых продуктах встречаются виды P. vulgaris, P. mirabilis, P. rettgeri, P. morganii. Представители этого рода признаны возбудителями пищевых токсикоинфекций. P. vulgaris – мелкие палочки размером (0,4–0,8) × (1–3) мкм, грамотрицательные, перитрихи, спор и капсул не образуют. Для рода Proteus характерен феномен «роения», приводящий к распространению в виде однородной пленки по влажной поверхности питательной среды. Proteus – факультативные анаэробы, не сбраживающие лактозу, большинство их штаммов ферментирует глюкозу с образованием кислоты и газа. Представителей рода выделяют не только из воды и почвы, но и из пищевых продуктов.
12.3.6. Vibrio parahaemolyticus
Случаи контаминации рыбы Vibrio parahaemoliticus – возбудителем гастроэнтеритов у человека были впервые описаны в 1951 г. в Японии. В дальнейшем Vibrio parahaemoliticus явился этиологическим фактором многочисленных вспышек гастроэнтеритов у жителей Азии, Америки, Европы. Парагемолитические вибрионы встречаются главным образом в прибрежных морских водах, в морской рыбе, крабах, моллюсках. Установлена следующая циркуляция этого вибриона: морская вода → рыба → человек → сточная вода → морская вода. Поскольку V. parahaemoliticus неустойчив и быстро погибает при тепловой обработке, холодильном хранении или замораживании, заражение этим микробом вероятно лишь в тех странах, где потребляют сырые продукты моря. Содержание V. parahaemoliticus нормируется в ряде рыбных и морепродуктов. В продуктах, не предназначенных для тепловой обработки, допускается не более 10 КОЕ/г; в сырой рыбе и моллюсках – не более 100 КОЕ/г.
Enterobacter sakazakii. Является причиной неонатального некротического энтероколита, неонатального менингита и сепсиса. Путь распространения – сухие молочные смеси. Бактерия считается условно-патогенной, однако отдельные штаммы токсичны для мышей-сосунков.
Е. sakazakii был выделен из неиспользованной готовой молочной смеси и неоткрытых банок отдельной партии. Из 141 образца сухой молочной смеси, полученного из 35 стран, 14% содержали Е. sakazakii. При бактериологическом исследовании питательных смесей в 6,7% из них обнаружили Е. sakazakii.
Е. sakazakii более термоустойчива, чем другие грамотрицательные бактерии. Допустимый уровень содержания Е. sakazakii в детских питательных смесях равен 1 КОЕ/100 г сухого вещества.
Повышенную устойчивость Е. sakazakii связывают с наличием трегалозы в бактерииальной клетке.
Бифидобактерии. Впервые бифидобактерии выделил в 1908 г. Tissieur. Он дал им название Bacillus bifidus. Этот вид был обнаружен исследователем во всех изучаемых пробах, взятых из стула детей. Позже Bacillus bifidus переименовали в Lactobacillus bifidus; ныне он квалифицирован как Bifidobacterium bifidum.
Аналогичные результаты, подтверждающие частоту встречаемости бифидобактерии в стуле человека, получены другими исследователями. Результаты многих исследований стали поводом для использования этих грамположительных анаэробных организмов в качестве индикаторов фекального загрязнения продуктов питания, в том числе вод.
Род Bifidobacterium включает в себя более 30 видов неподвижных палочковидных бактерий, не проявляющих каталазной активности. По современной классификации В. longum infantis, В. longum longum, В. longum suis считаются подвидами вида В. longum, а В. animalis animalis и В. animalis lactis – подвидами вида В. animalis.
Установлено, что В. bifidum с высокой частотой встречались у людей всех возрастных групп, но наибольшей частота их встречаемости была чаще всего у грудных детей (80,5%).
В. breve были обнаружены только у детей до 6 лет, а в группе подростков 12–15 лет бактерии этого вида обнаружены не были. Наиболее физиологичный для детей грудного возраста вид В. infantis встречался только у 14,2% детей в группе до 6 мес. Частота встречаемости В. adolescentis составляла более 30% во всех возрастных группах. Вид В. angulatum не был обнаружен у детей до одного 1 мес, в дальнейшем у детей 3–6 мес. и 12–24 мес. бактерии этого вида обнаружены с частотой 7,8 и 9,5% соответственно. Частота обнаружения В. angulatum составила: 8,2% у детей 4–6 лет и 11,5% у подростков 12–15 лет. Обращает на себя внимание довольно высокий уровень обнаружения В. dentium у грудных детей (22%) и детей-подростков (26,9%).
По данным ряда авторов, В. dentium является единственным оппортунистическим микроорганизмом рода Bifidobacterium. Он был обнаружен в высоких титрах в дентине кариозных повреждений у детей и вызывал кариес зубов. Этот вид обладает более высокой, чем у других бифидобактерии, биохимической, катаболистической, ферментативной, адгезивной активностью, что способствует его выживанию в полости рта. Обнаружение В. dentium в кишечнике может свидетельствовать о высоком риске развития кариеса у детей.
Таким образом, при изучении видового состава кишечных бифидобактерий было выявлено, что у детей до двухлетнего возраста доминирующими таксонами являются бифидобактерии видов В. bifidum, В. longum и В. catenulatum, а также В. adolescentis и В. breve. У детей 6 лет и у подростков бифидофлора в основном была представлена видами В. bifidum, В. catenulatum, В. longum, В. adolescentis и B.dentium.
Температурный оптимум роста этого рода микроорганизмов лежит между 25–28 и
43–45°С. Для роста бифидобактерии необходимы парааминобензойная и пантотеновая кислоты. Лучше всего они растут при рН среды от 5 до 8 и производят уксусную и молочную кислоты, являющиеся для них основными конечными продуктами метаболизма углеводов. Дифференциально-диагностическая среда Блаурока считается наиболее оптимальной. Бифидобактерии синтезируют витамины группы В (В1; В2 и др.) и витамин К.
Большая часть бифидобактерии располагается в толстой кишке, являясь ее основной пристеночной и просветной микрофлорой. В. bifidum, В. longum longum и В. longum infantis в общей сложности достигают 108–1011 КОЕ на 1/г содержимого толстой кишки. Они образуют большинство кишечной микрофлоры и обеспечивают колонизационную резистентность, ферментативную, антитоксическую, иммунную, метаболическую и другие функции толстой кишки. Непосредственно контактируя с энтероцитами, бифидобактерии (как и лактобактерии) стимулируют механизмы защиты организма человека, в том числе увеличение скорости регенерации слизистой оболочки, влияют на синтез антител к родственным, но обладающим патогенными свойствами микроорганизмам, активируют фагоцитоз, а также синтез лизоцима, интерферонов и цитокинов.
Бифидобактерии составляют 80–90% кишечной флоры детей, находящихся на грудном вскармливании, и молодняка млекопитающих в подсосном периоде. Присутствие бифидобактерии в кишечнике полезно для детей и молодых животных, так как бифидобактерии подавляют развитие различных гнилостных и болезнетворных микроорганизмов, способствуют перевариванию углеводов. По окончании молочного вскармливания бифидофлора сменяется обычной кишечной микрофлорой, характерной для взрослых организмов.
Из живой культуры бифидобактерии изготавливают лекарственные препараты, используемые для нормализации микрофлоры кишечника и противодиарейной терапии. Живые бифидобактерии обладают высокой антагонистической активностью против широкого спектра патогенных и условно-патогенных микроорганизмов кишечника (включая стафилококки, протеев, энтеропатогенную кишечную палочку, шигеллы, некоторые дрожжеподобные грибы), восстанавливают равновесие кишечной и влагалищной микрофлоры, нормализуют пищеварительную и защитную функции кишечника, активизируют обменные процессы, повышают неспецифическую резистентность организма.
Бактерии рода Yersinia. Род назван в честь Александра Йерсена – швейцарского бактериолога, открывшего его. Из всех представителей рода Yersinia самый опасный вид Yersinia pestis – возбудитель антропозоонозной чумы. В пищевых продуктах нередко обнаруживается Yersinia enterocolitica. Как и листерии, этот вид подвижен при температурах менее 30°С, а при 37°С и выше утрачивает подвижность.
Эти бактерии дают негативную реакцию на оксидазу, сбраживают глюкозу, не образуют газа и являются психрофилами. Успешное культивирование Yersinia enterocolitica удается при 2–45°С, при оптимуме в пределах 22–29°С. Отмечен рост отдельных штаммов при температуре 0–2°С после 20 сут инкубации в молоке. В молоке Yersinia enterocolitica успешно размножаются при 4°С.
Yersinia enterocolitica широко распространена в природе. Yersinia intermedia и Yersinia frederiksenii выделяют из пресной воды, пищевых продуктов и редко изолируют от человека.
Носители иерсиний выделяют представителей этого рода Yersinia с мочой и калом. Чаще всего люди инфицируются иерсиниями при употреблении необеззараженнорго молока.
Многие дикие животные и птицы инфицированы бактериями Yersinia enterocolitica.
Бактерии рода Campylobacter. Род Campylobacter включает девять видов патогенных для человека кампилобактерий. Ведущими видами в патологии человека являются Campylobacter jejuni, С. coli, С. lari, реже – С. fetus подвида fetus.
В роду бактерий Campylobacter видом, имеющим первостепенную важность для гигиенического состояния продуктов питания, является Campylobacter jejuni subsp. jejuni (далее – Campylobacter jejuni). Они растут при температуре 42°С и восстанавливают нитраты. Campylobacter jejuni – вибрионы, моно- или биполярные лофотрихи. Campylobacter coli и Campylobacter intestinalis, как и Campylobacter jejuni, могут быть причиной диареи у человека, тем не менее Campylobacter jejuni – самый патогенный вид из всех представителей рода.
12.4. ПАТОГЕННЫЕ МИКРООРГАНИЗМЫ
В чистой культуре первого возбудителя сальмонеллеза Salmonella cholerae (прежнее название S. suipestifer), которого долгое время считали возбудителем чумы свиней, в 1885 г. выделил американский ветеринар Д.Э. Сальмон. Паратифом позже назвали заболевание людей, возбудителями которого являются S. paratiphy А и В, так как симптомы болезни сходны с брюшным тифом. Впоследствии массовые болезни животных, вызываемые сальмонеллами, также назвали паратифами. Однако это название устарело и заменено. Установлено, что S. paratiphy А и В патогенны только для человека, в то время как виды и разновидности, выделяемые от животных и птиц, вызывают токсикоинфещии у человека.
Сальмонеллы отнесены к семейству Enterobacteriaceae, трибу Escherichiae, роду Salmonella. Род сальмонелл включает 65 групп (более 2400 сероваров). Международный номенклатурный род Salmonella разделил на четыре подрода:
- S.kauffmanni. Включает бо́льшую часть патогенных для человека сальмонелл, серологических групп А, В, С, Д;
- S.salamae отличается от первого подрода способностью разжижать желатин и ферментировать малонит натрия;
- S.arizonae. Ферментирует лактозу, обнаруживается у птиц, рептилий, млекопитающих; в последние годы обнаруживается у человека при лихорадочных состояниях с явлениями диареи и гастроэнтерита;
- S.Houtenau. Сюда отнесены атипичные в биохимическом отношении сальмонеллы.
С учетом способности инфицирования человека сальмонеллы могут быть поделены на три группы.
Первая группа включает S. myphi, S. paratyphi A, S. paratyphi В, которые являются инфекционными только для человека. Эти виды из всех сальмонелл вызывают крайне опасные болезни людей. При этом тифоидная лихорадка имеет наиболее продолжительный инкубационный период, вызывает повышение температуры тела и приводит к большому количеству смертельных исходов.
Вторая группа Salmonella считается строго адаптированной к определенным хозяевам серовары (некоторые из них являются патогенными для человека и ими можно заразиться от пищевых продуктов). К ней относятся S. gallinarum (домашняя птица, дичь), S. dublin (крупный рогатый скот), S. abortus-equi (лошади), S. abortusovis (овцы) и S. choleraesius (свиньи).
Третья группа состоит из неадаптированных к конкретному виду животных сероваров, являющихся патогенными как для животных, так и для человека.
Индикаторными микроорганизмами для всей группы патогенных кишечных бактерий в настоящее время признаны сальмонеллы. Разработаны эффективные методы их индикации и идентификации. При этом присутствие сальмонелл соответствует наличию шигелл, которые выделяются значительно труднее. Не допускается наличие сальмонелл в 25 г (см3) многих пищевых продуктов, иногда – в 50–100 г (см3).
Сальмонеллы – мелкие палочки с закругленными концами длиной до 2 мкм, в основном большинстве подвижные, грамотрицательные, спор и капсул не образуют. Факультативные анаэробы. Оптимальная температура их роста – 37°С.
Для целей серотипирования виды и серовары сальмонелл размещены по группам, обозначаемым А, В, С и т.д., которые соответствуют схожести в содержанию одного или более О-антигенов.
Кроме О-антигенов, для дальнейшей классификации используются Н-антигены жгутиков. Жгутиковые антигены подразделяют на специфические и неспецифические. Антигены, входящие в группу специфической разновидности, являются общими лишь для весьма ограниченного числа видов и вариантов бактерий рода Salmonella, в то время как антигены групповой разновидности очень широко распространены среди нескольких различных видов. Любая культура бактерий Salmonella может состоять либо из микроорганизмов, принадлежащих только к одной из этих двух разновидностей, либо к обоим жгутиковым разновидностям.
Сальмонеллы могут расти на множестве различных питательных средах и способны образовывать видимые колонии в течение 24 ч при 37°С. Не ферментируют лактозу, сахарозу или салицин. Для наилучшего роста сальмонелл необходим рН в области между 6,6-8,2.
Сальмонеллы чрезвычайно широко распространены в природе, а млекопитающие и птицы являются их главными резервуарами. Сущность механизма пищевых отравлений сальмонеллами заключается в потреблении пищевых продуктов, обсемененных большим количеством патогенных микроорганизмов.
Среда обитания сальмонелл – желудочно-кишечный тракт домашних и диких животных, человека и насекомых. При употреблении человеком и другими животными неочищенной воды и продуктов питания, которые могут быть загрязнены насекомыми или любым другим путем, эти микроорганизмы вновь выбрасываются в окружающую среду с фекальными массами, и таким образом цикл повторяется.
Появление сальмонелл в готовом продукте – показатель антисанитарного состояния этого пищевого продукта и воздуха.
12.4.2. Listeria monocytogenes
В 1926 г. ученым Кембриджского университета (исследование возглавлял Д. Мюррей) удалось впервые выделить возбудителя из тканей, забранных у больных морских свинок и кроликов.
Уже в 1927 г. У. Пири предложил назвать недавно открытую группу микроорганизмов листериями (Listeria) в честь ученого Д. Листера, который в свое время изучал природу этого заболевания на территории Южной Африки. А уже в 1929 г. возбудитель был выделен из тканей человека. В 1940 г. родовое наименование было изменено на Listeria.
В последние десятилетия XX в. и по настоящее время были зарегистрированы эпидемические вспышки и спорадические случаи листериоза в высокоразвитых странах мира. Все вспышки были обусловлены употреблением пищевых продуктов: сыров, мясных полуфабрикатов, салатов и др.
Род Listeria разделен на шесть видов: L. monocytogenes, L. innocua, L. seeligeri, L. welshimeri, L. ivanovii, L. grayi. Типичным представителем рода Listeria является L. monocytogenes.
Вид L. monocytogenes представлен 13 сероварами, некоторые из которых разделяют также на виды L. innocua и L. seeligeri.
Серотипы листерий неразрывно связаны с определенным хозяином, определенным типом заболевания и географическим происхождением. Данное свойство листерий доказано путем выделения изолятов из продуктов питания, произведенных в различных странах мира для коммерческой реализации.
Листерии хорошо растут в сердечно-мозговом бульоне, триптиказно-соевом бульоне и триптозном бульоне. Для полноценного роста листерий необходимы четыре витамина группы В – биотина, рибофлавина, тиамина и тиоктовой кислоты (альфа-липоевая кислота; фактор роста для некоторых бактерий и простейших), а также аминокислоты (цистеин, глутамин, изолейцин, лейцин и валин). Глюкоза усиливает рост всех видов листерий, при этом вырабатывается молочная кислота. Кроме глюкозы, отдельные виды листерий потребляют другие простые и сложные углеводороды. Листерии напоминают многие виды энтерококков по способности гидролизовать эскулин и расти в присутствии солей желчных кислот в концентрации от 10 до 40%, а также 10% NaCl, 0,025% ацетата таллия и 0,04% теллурита калия. Однако в отличие от энтерококков листерии не могут расти в присутствии 0,02% азида натрия. Листерии обладают системой гидролаз желчных кислот, что позволяет им расти в желчном пузыре. В отличие от большинства других грамположительных бактерий листерии растут на агаре МакКонки.
Представители рода Listeria не имеют специфических железо-связывающих компонентов, хотя железо является важным элементом, необходимым для их роста. Поэтому механизм восстановительной мобилизации свободного железа, которое связывается с поверхностными рецепторами, является единственным источником удовлетворения потребности листерий в железе.
Листерии лучше всего растут при рН от 6 до 8. Как правило, минимальное значение рН роста является функцией температуры инкубации, состава питательных веществ и субстратов роста, активности воды (aw) и присутствия и концентрации NaCl и других солей или ингибиторов.
Средняя минимальная температура роста L. monocytogenes на триптиказном соевом агаре 1,1 ± 0,3°С с разбросом в пределах от 0,5 до 3,0°С. Максимальная температура роста листерий – около 45°С.
Листерии широко распространены в природе и обладают стойкостью к воздействию внешней среды. Они могут быть обнаружены в воде, почве, а также на растениях или трупах мертвых животных, испражнениях животных, канализационных водах, силосной массе. Эти бактерии легко переносят замораживание. Даже под воздействием прямых солнечных лучей листерии могут сохранять способность к жизнедеятельности на протяжении двух недель.
Как правило, листерии живут в тех средах обитания, где существуют молочнокислые бактерии, Brochothrix, а также некоторые виды из коринеформных бактерий. Связь бактерий этой группы с молочными продуктами и силосом хорошо известна, так же как и связь с этими продуктами некоторых других продуцентов молочной кислоты. Чаще всего бактерии L. monocytogenes и L. innocua обнаруживают в образцах вместе с бактериями L. seeligeri.
Любые свежие продукты питания животного и растительного происхождения могут содержать бактерии L. monocytogenes, L. innocua, L. welshimeri, L. grayi, L. seeligeri в тех или иных количествах. Эти организмы, как правило, выявляются в сыром молоке, мягких сырах, в свежем и замороженном мясе, яйце, морепродуктах, фруктовых и овощных продуктах.
12.5. АНТРОПОНОЗНЫЕ ЗАБОЛЕВАНИЯ
Антропонозы (антропонозные инфекции) (от др.-греч. νθρωποζ – человек, νóσοζ – болезнь) – группа инфекционных и паразитарных заболеваний, возбудители которых способны паразитировать в естественных условиях только в организме человека. Источником возбудителей инфекции антропонозов являются только больные люди – носители возбудителей инфекции/инвазии. В группу антропонозов, передающихся через пищевые продукты или воду, входят нозоформы: холера, брюшной тиф, дизентерия, паратифы А и В, вирусный гепатит.
Холера (от греч. cholera, от: chole – желчь, rheō – течь, истекать) – острое инфекционное заболевание, характеризующееся поражением кишечника, диареей, рвотой, быстрой потерей организмом жидкости. Из-за тяжелого течения болезни и возможности быстрого эпидемического и пандемического распространения согласно Международным медико-санитарным правилам холера относится к особо опасным инфекциям (ООИ).
Возбудитель холеры – Vibrio cholerae относится к семейству Vibrionaceae. По чувствительности к специфическому фагу различают два биотипа возбудителей – классический холерный вибрион Vibrio cholerae biovar cholerae и вибрион Эль-Тор (Vibrio cholerae biovar eltor). Vibrio cholerae представляет собой короткую прямую или изогнутую палочку размером (1,5–3,0) × (0,2–0,6) мкм, имеющую один полярно расположенный длинный жгутик, который обусловливает ее высокую подвижность. По Граму холерный вибрион окрашивается отрицательно, спор и капсул не образует. Под действием пенициллина холерный вибрион способен образовывать L-формы. Возбудитель образует термолабильный экзотоксин холероген. V. cholerae – строгий аэроб. Оптимальная температура роста – 37°С. Наиболее благоприятное значение рН среды 7,6–9,0. При снижении рН ниже 5,5 быстро гибнет. На жидкой среде растет в виде серой или голубоватой пленки. На плотной среде возбудитель образует небольшие дисковидные S-колонии с ровными краями, голубоватые в проходящем свете, что сразу отличает их от энтеробактерий.
В 1%-й пептонной воде с 0,5% хлорида натрия вибрионы вырастают за 6–8 ч, образуя слабую муть и нежную пленку на поверхности среды, в то время как другие микроорганизмы на этой среде вырастают только за 20–24 ч.
Холерный вибрион образует термостабильный эндотоксин (липопротеиновый комплекс) и термолабильный экзотоксин – энтеротоксин, или холероген, обусловливающий развитие основных патогенетических механизмов дегидратации и деминерализации организма человека. Устойчивость холерного вибриона во внешней среде относительно невелика. Он очень чувствителен к высушиванию, УФ-облучению, дезинфицирующим препаратам, высокой температуре. Во влажной среде при 56°С возбудитель погибает через 30 мин, при 60°С – через 10 мин, при кипячении – мгновенно. Вибрион чувствителен к слабым растворам кислот, но устойчив к щелочам. На мясных и рыбных продуктах вибрион Эль-Тор выживает 2–5 сут, на поверхности плодов и овощей – до 8 сут. В открытых водоемах возбудитель сохраняется несколько месяцев, под прямым солнечным светом – до 8 ч.
Резервуаром возбудителей служит больной холерой человек, переболевший человек или здоровый вибриононоситель, выделяющий возбудителя в окружающую среду с фекалиями и рвотными массами. Больной наиболее опасен в первые дни болезни, когда испражнения и рвотные массы содержат наибольшее количество возбудителя. Весьма опасны больные с легкими формами заболевания, поскольку их трудно выявить. Заболевание распространяется также через воду, пищевые продукты и контактно-бытовым путем. Кроме того, холерные вибрионы могут переноситься мухами. В последние годы стало известно, что возбудитель холеры Эль-Тор способен сохраняться в организмах простейших, рыб, ракообразных и других обитателей водоемов.
Ключевую роль в профилактике заболеваемости холерой играют общие санитарные меры, такие как: обеспечение населения доброкачественной питьевой водой, обезвреживание сточных вод, коммунальное благоустройство. При возникновении очагов заболевания главными профилактическими мероприятиями являются госпитализация больных, изоляция и проведение обследований лиц, находившихся в контакте с больными. Важно в полном объеме выполнять меры по предупреждению и максимальной защите от заноса и распространения холеры из-за рубежа. В России создано более 270 санитарно-карантинных пунктов пропуска через границу в речных и морских портах, аэропортах, на автодорожных переездах. Необходимо проводить санитарно-бактериологическое обследование граждан, заболевших за рубежом острыми кишечными инфекциями, а также осуществлять медицинское наблюдение в течение 5 сут за лицами, прибывшими из районов, неблагополучных по холере. Для специфической профилактики с 7-летнего возраста применяют пероральную противохолерную вакцину, которую вводят начиная с семилетнего возраста. Людей, переболевших холерой, допускают к работе на пищевых предприятиях только с разрешения медицинской комиссии.
Дизентерия (от греч. dysenteria, где: dys – приставка, означающая нарушение, enteron – кишка) – острое инфекционное заболевание, характеризующееся поражением желудочно-кишечного тракта, преимущественно толстой кишки, и протекающее с явлениями общей интоксикации. В честь К. Шига дизентерийные бактерии получили родовое название Shigella. Исследования С. Флекснера (1900 г.), К. Зонне (1915 г.), Дж. Бойда (1932 г.) позволили выделить новые виды шигелл.
Возбудители бактериальной дизентерии относятся к семейству Enterobacteriaceae, роду Shigella. В соответствии с антигенной структурой и биохимическими свойствами более 50 известных вариантов шигелл разделены на виды: Shigella dysenteriae, Shigella flexneri, Shigella sonnei.
Возбудитель дизентерии – короткая палочка с закругленными концами размером
(0,5–0,7) × (1,0–3,0) мкм. Палочки неподвижны, грамотрицательны, спор не образуют. Возбудители дизентерии являются факультативными анаэробами. Оптимальная температура их роста составляет 37°С (при температуре выше 45°С рост прекращается), оптимальное значение pH среды – 6,8–7,2. На плотных средах шигеллы вырастают в виде мелких прозрачных колоний. Средой обогащения для выделения и культивирования шигелл является селенитовый бульон.
Патогенность возбудителей определяется способностью к образованию экзотоксинов (в том числе шигатоксина), обладающих энтеротоксической активностью, эндотоксина (липополисахаридного комплекса – ЛПС-комплекса), цитотоксинов и нейротоксинов.
Возбудители дизентерии могут сохраняться в почве, пищевых продуктах, на различных предметах в течение 10–15 сут. При нагревании до 60°С они погибают через 10 мин, при кипячении – мгновенно. В растворах хлорамина, хлорной извести гибель шигелл
наступает через 5–6 мин, под воздействием прямого солнечного света – через 20–30 мин. Шигеллы Зонне способны размножаться и накапливаться в пищевых продуктах, особенно в молоке и молочных продуктах. В процессе гибели шигелл в контаминированных пищевых продуктах накапливается термостабильный ЛПС-комплекс, способный вызывать тяжелые поражения кишечника при отрицательных результатах бактериологического исследования этих продуктов. ,
Резервуаром и источником шигелл является больной человек или бактерионоситель возбудителя. Из организма человека шигеллы начинают выделяться при первых симптомах заболевания; продолжительность выделения – 7–10 сут. Иногда выделение бактерий затягивается до нескольких недель или месяцев. Механизм передачи дизентерии – фекально-оральный. Пути передачи – водный, пищевой и контактно-бытовой. Промежуточным переносчиком могут являться мухи. Заболевание начинается с общего недомогания, повышения температуры до 39°С, озноба. Появляются боли в животе, сначала постоянные, затем принимающие схваткообразный характер. Стул становится частым, выделения содержат патологические примеси: кровь, гной, слизь. Дальнейшее течение болезни зависит от тяжести заболевания, сопротивляемости организма, методов лечения. Выраженная вирулентность, наличие у отдельных штаммов шигелл лекарственной устойчивости обусловливают способность этих микроорганизмов вызывать массовые заболевания в виде крупных эпидемий с тяжелым течением заболевания.
Профилактические меры включают своевременное выявление больных и бактерионосителей, раннюю госпитализацию и лечение, санитарный надзор за пищевыми предприятиями, повышение санитарной культуры населения. В очагах инфекции с профилактической целью может быть использован дизентерийный бактериофаг. Все поступающие на пищевые предприятия лица подвергаются однократному бактериологическому обследованию. При выделении у данных лиц возбудителей дизентерии и других кишечных заболеваний их не допускают к работе и направляют на лечение.
12.5.3. Брюшной тиф и паратифы А и В
Брюшной тиф (от греч. typhos – туман) – это острая кишечная инфекция, характеризующаяся лихорадкой, головной болью, симптомами общей интоксикации с развитием тифозного статуса, что проявляется заторможенностью, нарушением сознания, бредом, галлюцинациями. Через 6–7 сут циркулирующие в лимфатических узлах бактерии погибают, а при разрушении освобождают эндотоксин. На 8–10-е сут у больных появляется розеолезная сыпь с преимущественной локализацией на животе. Во время болезни отмечаются значительное повышение температуры, расстройство сердечно-сосудистой деятельности, работы центральной нервной системы. Увеличиваются печень и селезенка, поражается лимфатическая система тонкого кишечника. Возможны осложнения в виде перфораций кишечника с последующим перитонитом и кровотечением.
Возбудитель брюшного тифа – Salmonella enterica. Серовар S. typhi (семейство Enterobacteriaceae) был открыт К. Эбертом в 1880 г. Родовое название Salmonella дано этим бактериям в честь американского ученого Д. Сальмона. Род Salmonella включен в отдел Gracilicutes, семейство Enterobacteriaceae.
Сальмонеллы – мелкие прямые палочки с закругленными концами размером
(0,3–0,5) × (1–30) мкм, грамотрицательные, подвижные (перитрихи). У некоторых сероваров жгутики отсутствуют (S. gallinarum, S. pullorum). Сальмонеллы не образуют эндоспор, только три серовара обладают микрокапсулой (S. typhi, S. paratyphi, S. dublin).
Сальмонеллы – факультативные анаэробы. Расщепляют глюкозу и другие углеводы с образованием кислоты и газа (за исключением S. typhi). На МПА они образуют мелкие колонии диаметром 1–4 мм, прозрачные, имеют голубой цвет. Сальмонеллы хорошо растут на среде Эндо – розоватые, полупрозрачные; на среде Плоcкирева – коричневые; на висмут-сульфитном агаре – черные с металлическим блеском. Оптимальная температура их размножения – 35–37°С; pH среды – 6,5–7,5.
Сальмонеллы во внешней среде могут не только сохранять свою жизнеспособность, но и активно размножаться. В воде они сохраняют свою жизнеспособность от 1 до 5 мес, на овощах и фруктах – до 10 сут, в колбасных изделиях – от 60 до 130 сут, в куриных яйцах – до 13 мес. При воздействии 3%-го раствора хлорамина, 5%-го раствора фенола, 95%-го спирта их гибель наступает через несколько минут.
Резервуаром и источником инфекции служит больной человек или бактерионоситель. В инкубационном периоде заболевания зараженный человек практически не опасен с точки зрения распространения болезни. Максимальное выделение возбудителя с фекалиями и мочой отмечается на 2–3-й неделе заболевания, Возбудителя можно также обнаружить в грудном молоке и носоглотке. Особая опасность в этом отношении исходит от носителей, работающих на пищевых производствах, предприятиях общественного питания, в продовольственных магазинах, детских учреждениях. Механизм передачи заболевания – фекально-оральный, он реализуется водным, пищевым и бытовым путями. Из пищевых продуктов наиболее опасны молоко и молочные продукты, кремы, салаты. Иногда заражение может произойти и через овощи, особенно при их поливе сточными водами.
Профилактические мероприятия включают выявление бактерионосителей брюшно-тифозной палочки и пресечение путей передачи инфекции. Большое значение имеют санитарное просвещение населения, знание и применение работниками общественного питания и торговли пищевыми продуктами установленного санитарного минимума.
Паратифы А и В. Возбудители паратифов S. paratyphi А и S. paratyphi В по морфологическим и культуральным свойствам сходны с Salmonella typhi. Паратиф А, в отличие от брюшного тифа, протекает в среднетяжелой форме и в начальном периоде сходен с острыми респираторными заболеваниями. Сыпь, более обильная, чем при тифе, появляется приблизительно на 4–7 сут болезни. Для паратифа В характерны симптомы гастроэнтерита, возникающие с первых дней заболевания. Сыпь может иметь разнообразный характер и располагаться не только на теле, но и на конечностях.
Основными мероприятиями профилактики являются: обеспечение населения доброкачественной водой, строгий санитарный контроль качества пищевых продуктов и условий их хранения, выявление больных и бактерионосителей, правильная система удаления нечистот. Для лечения применяют антибиотики: левомицетин, ампициллин, бисептол и др.
Вспомогательное значение имеет иммунизация, проводимая по эпидемиологическим показаниям среди населения, начиная с трех лет, в местностях, не благополучных по брюшному тифу (уровень заболеваемости > 25 случаев на 100 тыс. населения).
12.6. ПИЩЕВЫЕ ОТРАВЛЕНИЯ МИКРОБНОГО ПРОИСХОЖДЕНИЯ
Пищевые отравления микробной этиологии подразделяют на токсикоинфекции, токсикозы и микотоксикозы (табл. 12.4).
Таблица 12.4
Возбудители пищевых отравлений
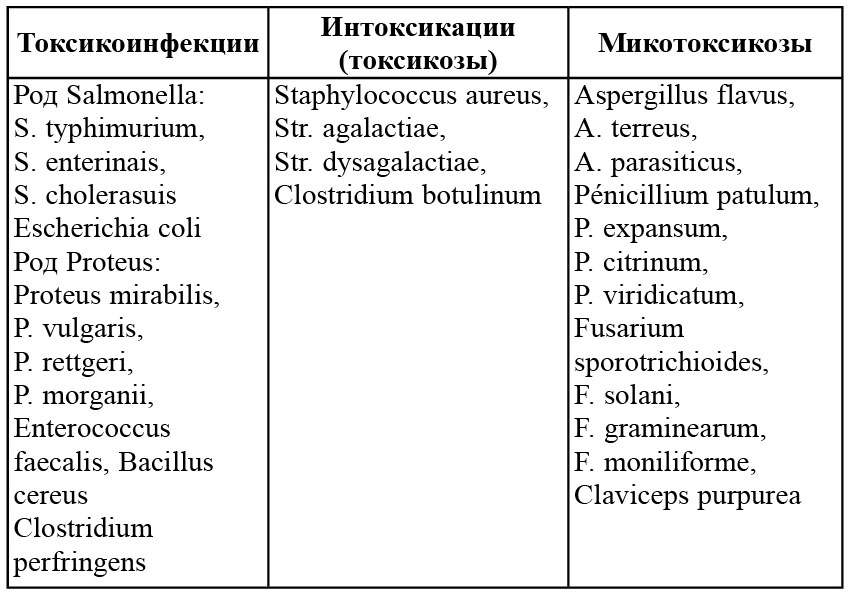
12.6.1. Пищевые токсикоинфекции
Токсикоинфекции – острые заболевания, возникающие в результате употребления в пищу продуктов, в которых размножились условно-патогенные микроорганизмы. Попадающие с пищей в желудочно-кишечный тракт человека микроорганизмы разрушаются, в результате чего высвобождаются эндотоксины, которые вызывают патологические изменения в стенке кишечника и оказывают токсическое действие на центральную нервную систему.
Эндотоксины бактерий. Грамотрицательные бактерии обладают двуслойной клеточной стенкой, которая окружает цитоплазматическую мембрану. Первый слой – очень тонкая (толщиной 1 нм) нелипидная мембрана, состоящая из пептидогликана. Его называют также гликопептидом или мукопептидом. Это сложный матрикс, содержащий полисахаридные цепи, связанные друг с другом поперечными сшивками из коротких пептидных цепей. Второй слой клеточной стенки – липидная мембрана толщиной 7,5 нм. Именно на этой внешней мембране и расположены эндотоксины (липополисахариды).
Молекулы эндотоксина формируют у бактерии структурную целостность, определяют антигенность и патогенность бактерий (рис. 12.1).
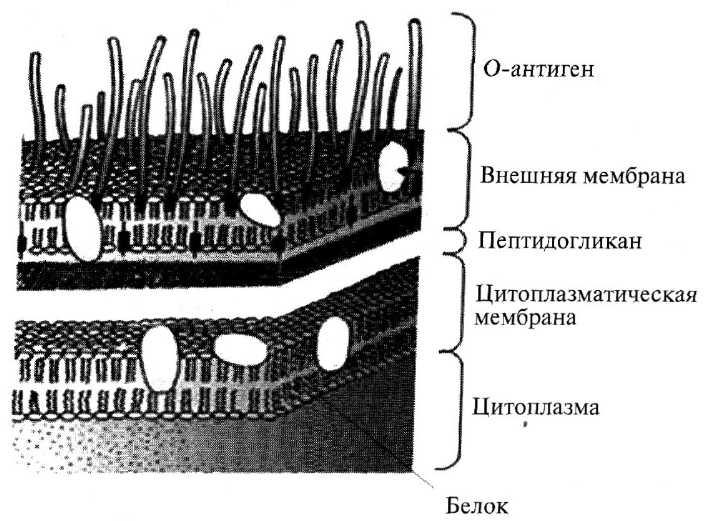
Рис. 12.1.
Структура клеточной стенки грамотрицательных бактерий
Структурно молекула эндотоксина делится на три части – липид А, кор и О-специфическую цепь (рис. 12.2).
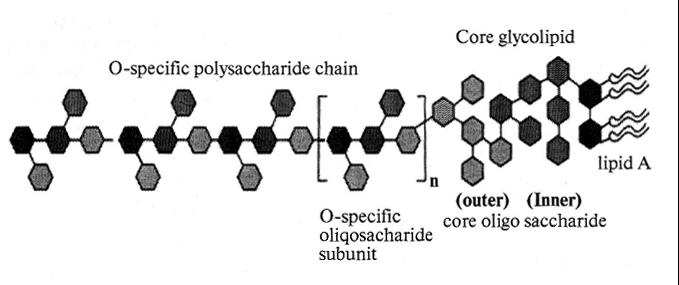
Рис. 12.2.
Структура молекулы эндотоксина (липополисахарида)
ЛПС построена из повторяющихся олигосахаридов. Наиболее распространенными сахарами, входящими в состав О-специфической цепи, являются глюкоза, галактоза, рамноза. Этот участок молекулы придает ей гидрофильные свойства, благодаря которым ЛПС хорошо растворимы в воде. Полисахаридная часть является наиболее вариабельной частью молекулы ЛПС. Часто этот фрагмент молекулы называют О-антигеном, так как именно он отвечает за антигенную активность грамотрицательных бактерий.
Кор – центральная часть молекулы, связывающая О-антиген с липидом А. Формально структура кора подразделяется на внешнюю и внутреннюю части. В состав внутренней части кора обычно входят остатки L-глицеро-О-манногептозы и 2-кето-З-дезоксиоктоновой кислоты (КДО). КДО содержит 8 атомов углерода и в природе практически нигде больше не встречается.
Липид А состоит из дисахарида, фосфата и жирных кислот. Участок липида А является наиболее константным участком молекулы ЛПС, а его строение схоже у многих бактерий.
В состав клеточной стенки грамотрицательных бактерий входят и белки (внешняя мембрана на 3/4 состоит из ЛПС и только 1/4 приходится на белковые компоненты). Вместе с ЛПС они образуют белково-липополисахаридные комплексы. Именно эти комплексы и называются бактериальными эндотоксинами, которых у отдельных микробных клеток насчитывается до 3,5 млн молекул. Очищенные препараты эндотоксинов, которые используются в качестве стандартов, лишены пептидных фрагментов и представляют собой чистый препарат ЛПС. Тем не менее термин «бактериальные эндотоксины» применяется с равным успехом и к естественным эндотоксинам, оказавшимся в растворе в результате разрушения бактерий, и к чистым препаратам ЛПС.
Эндотоксины грамотрицательных бактерий остаются биологически активными молекулами и после гибели бактерий. Молекула эндотоксина термостабильна и легко выдерживает цикл стерилизации в автоклаве. Малые размеры молекул эндотоксинов позволяют им легко проходить через мембраны, используемые для стерилизации растворов (0,22 мкм). Поэтому эндотоксины могут присутствовать в готовых лекарственных формах, даже произведенных в асептических условиях и прошедших финишную стерилизацию.
Бактериальные эндотоксины являются исключительно активными (сильными) пирогенами. Для развития лихорадочного приступа достаточно присутствия бактериальных эндотоксинов в инфузионном растворе в концентрации 1 нг/мл. Другие пирогены менее активны, и для развития пирогенного ответа их концентрация должна быть в 100–1000 раз больше. Обычно термины «пирогены» и «эндотоксины» употребляются как синонимы. Хотя не все пирогены являются эндотоксинами, наиболее значимыми являются именно эндотоксины грамотрицательных бактерий.
Порообразующие токсины. К ним относят бактериальные токсины, функционирующие посредством вставки в плазматическую мембрану хозяина и формирующие в ней трансмембранные поры, приводящие клетку к лизису. Такие токсины еще называют RTX-семейством из-за наличия в их молекулах большого количества повторов. Механизм их действия хорошо прослеживается на примере альфа-токсина S. aureus, рассматриваемого как прототип олигомеризующегося пороформирующегося цитотоксина.
Организация и механизм действия токсической молекулы. Большинство токсинов представляют собой А–B-структуру, которая предполагает наличие двух компонентов – В-субъединицы, которая участвует в связывании токсина с рецептором на поверхности клетки хозяина и способствует транспортировке токсина в клетку хозяина, и А-субъединицы, проявляющей энзиматическую (токсическую) активность в клетке хозяина. Структура В-доменов зависит от структуры рецепторов-мишеней, с которыми взаимодействует токсин. А-субъединицы более консервативны, чем В, особенно на участках, критических для их ферментативной активности.
Сальмонеллы. Наиболее частыми среди пищевых токсикоинфекций (96 % случаев) являются сальмонеллезы, вызываемые бактериями рода Salmonella. Возбудителями пищевых токсикоинфекций являются, как правило, S. typhimurium, S. enteritidis, S. cholerasuis.
Сальмонеллы могут длительное время сохраняться в различных пищевых продуктах. В сливочном масле они сохраняли жизнеспособность в течение 4 мес при комнатной температуре и в течение 9–10 мес в условиях холодильного хранения. В замороженном меланже при температуре –20°С сальмонеллы могут выживать в течение 13 мес. В мороженом мясе сальмонеллы обнаруживались после 2–3 лет хранения, в соленом мясе – до 5–6 мес. Основной причиной сальмонеллезных токсикоинфекции является употребление мяса и мясных продуктов. Около 70% случаев сальмонеллезных токсикоинфекции вызывается мясными продуктами от вынужденно забитых животных. Мясо может быть инфицировано как при жизни животного, так и посмертно. Контаминация мяса и мясных изделий сальмонеллами может происходить при контакте с грязными руками, грызунами, мухами. Сальмонеллы размножаются в мясе и мясных продуктах, рыбе и рыбопродуктах, молоке и молочных продуктах и не изменяют органолептических свойств этих продуктов.
Особую опасность представляют студни, состав и технология производства которых способствуют контаминации сальмонеллами. Причиной вспышек сальмонеллеза могут быть также низкосортные колбасы (ливерные и кровяные), зельцы, мясные и печеночные паштеты, макароны «по-флотски». Молоко и молочные продукты (сыр, сметана, мороженое) находятся на втором месте как фактор передачи возбудителя сальмонеллеза (около 10% случаев). Примерно 8–10% случаев сальмонеллеза связаны с употреблением яиц, яичного меланжа и майонеза. До 3% отравлений приходится на рыбные продукты, единичные вспышки могут быть обусловлены употреблением салатов, винегретов, кондитерских изделий с кремом.
Патогенные кокки (от греч. kokkos – зерно). Они относятся к отделу Firmicutes, классу Schysomicetales, семействам Micrococacceae, Diplococcaceae и родам Staphylococcus и Streptococcus.
Кокки широко распространены в природе. Они обитают на слизистых и кожных покровах, на растениях, в молочной железе, высокоустойчивы к неблагоприятным факторам и чувствительны к анилиновым красителям. Кокки обладают токсичностью. Некоторые из них, особенно стафилококки, являются условно патогенными. Они обладают органотропностыо.
Биологические особенности патогенных кокков весьма разнообразны:
- кокки различных видов вызывают аналогичные инфекционные процессы, сопровождающиеся нагноением;
- кокки одинакового вида часто являются причиной различных инфекционных процессов – от местного воспаления до множественных абсцессов и сепсиса;
- у части видов значительно выражена органотропность (диплококки чаще других видов вызывают пневмонию, мытный стрептококк – воспаление шейных лимфоузлов и протоков; менингококки – воспаление оболочек спинного и головного мозга у человека);
- кокки нередко обусловливают кормовые и пищевые токсикоинфекции;
- все патогенные кокки в большей или меньшей степени токсичны;
- патогенные кокки вызывают множество заболеваний;
- патогенные кокки участвуют в проявлении ассоциативных инфекций, вызванных
Е. coli, клостридиями, Р. vulgaris.
Кокки являются грамположительными бактериями (кроме менингококков и возбудителя гонореи) размером от 0,2–0,4 до 4,0– 4,5 мкм, имеют шаровидную форму, не образуют спор, неподвижны, располагаются в виде скоплений стафилококков, монококков и стрептококков.
Культивирование. Для роста на питательных средах кокки нуждаются в добавлении крови (плазмы крови) или асцитической жидкости, глюкозы.
Кокки анаэробы (факультативные анаэробы) растут на обычных питательных средах (МПА, МПБ) при температуре 35–40°С и при рН от 7,0 до 7,5.
Большинство кокков отличается высокой биохимической активностью как к сахарам, так и белкам. Они вызывают разнообразные болезни животных и птиц.
Стафилококки. В настоящее время различают S. aureus, S. epidermidis и S. saprophyticus. Из трех видов патогенным является Staphilococcus aureus.
В патологии животных этиологическая роль стафилококков за последнее время значительно возросла. Эти микробы часто вызывают мастит, послеродовой эндометрит у коров, пневмонию, септицемию, энтерит у молодняка, абсцессы, флегмоны, артриты, гнойные воспаления ран. У кур данный микроб является возбудителем септического заболевания – стафилококкоза, сопровождающегося массовой гибелью птицы.
У лошадей, свиней и реже у крупного рогатого скота стафилококки обусловливают развитие ботриомикоза, характеризующегося формированием в семенном канатике после кастрации гнойных очагов, окруженных плотной капсулой.
Устойчивость стафилококков к неблагоприятным факторам внешней среды высокая. Они превосходно переносят высыхание, оставаясь жизнеспособными в гнойном экссудате до 200 сут, длительно сохраняются в навозе, замораживание их консервирует. На питательных средах, в частности на полужидком агаре, сохраняются без пересевов более
6 мес. При нагревании, например в молоке, погибают при температуре 70°С через 1 ч, при 85°С – через 30 мин, кипячение убивает их мгновенно. При дезинфекции 1%-й раствор формалина и 2%-й раствор едкого натра убивают этих микробов в течение 1 ч, а 1%-й раствор хлорамина – в течение 2–5 мин. Наиболее чувствительны стафилококки к кристаллвиолету, пиоктанину, малахитовой зелени, которые в концентрации 1: 300 000 обладают выраженным бактериостатическим действием, что позволяет с успехом использовать эти краски при стафилококковых поражениях кожи, фурункулезе, нагноении ран. Весьма устойчивы стафилококки к антибиотикам, особенно пенициллину, стрептомицину, а также сульфаниламидным препаратам. Учитывая высокую устойчивость стафилококков, их используют в качестве тест-объектов при испытании различных бактерицидных веществ – новых антибиотиков или дезинфицирующих веществ.
Санитарно-показательный вид. Так как основным источником обсеменения сборного молока стафилококками является молоко, полученное от коров, больных маститом, необходимо выявлять больных животных, особенно с субклиническими формами маститов, и не допускать смешивания маститного и сборного молока.
Стафилококковые пищевые отравления возникают при употреблении различных продуктов. Часто они вызываются молочными и мясными продуктами. Известны случаи отравления при употреблении кондитерских изделий, особенно с заварным кремом и сметаной; рыбных и мясных салатов и других пищевых продуктов, зараженных токсическими стафилококками. Обычно такие продукты не имеют внешних признаков порчи.
Источником обсеменения продуктов питания патогенными стафилококками могут быть люди с гнойничковыми поражениями кожи (фурункулами, абсцессами, нагноившимися ранами и царапинами), а также больные ангиной и имеющие токсигенные стафилококки в носоглотке и в верхних дыхательных путях. Пища может обсеменяться (инфицироваться) стафилококком через капельки слюны, выделяемой при кашле, чихании, а также при непосредственном соприкосновении с руками. Такие люди не должны допускаться к работе на пищевых предприятиях.
Признаки отравления появляются обычно в виде острого желудочно-кишечного заболевания через 1–6 ч после приема зараженной пищи.
Токсигенность. Патогенные кокки продуцируют гемотоксин различного действия: альфа-, бета-, гамма-, дельта-гемолизин. Лейкоцидин вызывает дегрануляцию и разрушение лейкоцитов и угнетает их фагоцитарные свойства. Стафилококки образуют энтеро-токсины – термостабильные пептиды, которые вызывают кормовые и пищевые токсикозы.
Кроме экзотоксинов, кокки продуцируют ферменты патогенности: гиалуронидазу, фибринолизин, дезоксикарбоксилазу и др.
Основная роль в патологии животных и человека принадлежит S. aureus, реже S. epidermidis, S. equi, S. pyogenes, S. agalactiae, S. pneumoniae.
Патогенные кокки проявляют свое патогенетическое действие чаще всего в ослабленном организме и при иммунодефицитных состояниях. Характер патогенетического процесса зависит как от вирулентности возбудителей, так и от уровня неспецифических факторов защиты организма.
Кокки проникают в организм через поврежденную кожу, слизистые оболочки, алиментарно, у коров – через сосковый канал. Возбудители за счет высокой токсичности и действия ферментов патогенности вызывают местную воспалительную реакцию, чаще гнойного типа, а также септический процесс.
Впервые выделил их и определил их патогенность для человека Луи Пастер в 1880 г. Они относятся к семейству Streptococcaceae, роду Streptococcus.
Род представлен 38 видами, которые подразделены на четыре условные группы: пиогенные, или гноеродные (Str. pyogenes, Str. agalactiae, Str. dysagalactiae, Str. equi и др.; всего 8 видов); стрептококки ротовой полости (Str. pneumoniae, Str. oralis, Str. anginosus и др.; всего 18 видов); анаэробные стрептококки (Str. hansenii, Str. morbillosum, Str. parvulus и Str. pieomorpbus) и группа «другие стрептококки» (Str. thermophilis, Str. uberis, Str. bovis, Str. acidominimus и др.; всего 8 видов).
Патогенные стрептококки чаще обусловливают маститы (Str. agalactiae, Str. dysagalactiae), гнойно-воспалительные процессы, сепсис (Str. pyogenes), острые и хронические инфекционные болезни (Str. equi, Str. pneumoniae).
Причиной пищевых токсикозов являются в основном возбудители маститов. Патогенные стрептококки образуют такие же токсины, что и патогенные стафилококки, однако пищевые токсикозы стрептококковой этиологии встречаются крайне редко.
Стрептококки плохо растут на обычных питательных средах. Их культивируют на средах с добавлением сыворотки крови и глюкозы. На МПА вырастают точечные беспигментные прозрачные колонии, в МПБ образуется небольшое помутнение и осадок.
На кровяном агаре отдельные штаммы стрептококков (Str. equi, Str. pyogenes) образуют вокруг колоний прозрачную зону гемолиза (b-гемолиз). Возбудитель пневмонии (Str. pneumoniae) образует вокруг колоний зеленовато-серую зону просветления (a-гемолиз). Отдельные штаммы Str. dysagalactiae оказываются негемолитичными (γ-гемолиз).
Патогенные стрептококки проявляют минимальную биохимическую активность по сравнению с сапрофитами. Они относительно резистентны: в высушенном состоянии могут сохраняться в течение 4–6 мес. Под действием прямых солнечных лучей погибают через 2–3 ч, 3–5%-й раствор фенола, 2%-й раствор формалина убивают стрептококки через 15 мин. При кипячении они погибают немедленно, режимы пастеризации молока обезвреживают патогенные стрептококки.
Источником пищевых отравлений стрептококковой этиологии могут служить продукты, полученные от животных, больных маститом и септицемией, а также продукты питания, загрязненные лицами, имеющими гнойничковые заболевания. Поэтому средства и методы профилактики стрептококковых интоксикаций те же, что и стафилококковых токсикозов.
Ботулизм. Ботулизм – это тяжелое пищевое отравление, возникающее при употреблении продуктов питания, содержащих экзотоксин Clostridium botulinum, и часто заканчивающееся летальным исходом. Документально заболевание ботулизмом было зафиксировано в 1793 г., когда в Вюртемберге заболели 13 человек, употребивших в пищу кровяную колбасу, из которых шесть умерли. В 1817–1822 тт. немецкий врач Ю. Керн сделал клинико-эпидемиологическое описание заболевания. Отравление возникло после употребления в пищу колбасы, поэтому отравление «колбасным» ядом исследователь назвал ботулизмом (от лат. botulus – колбаса). В России эта болезнь была неоднократно описана в XIX в. в связи с употреблением соленой и копченой рыбы, на основании чего получила название «ихтиизм». В 1894 г. в Бельгии 34 музыканта отравились ветчиной домашнего приготовления, из которой бактериолог Э. Ван-Эрменгем выделил возбудителя ботулизма. В Западной Европе ботулизм был связан с употреблением колбасных изделий, в Америке – овощных консервов, в России – красной рыбы. Болезнь начинается остро, появляются тошнота, рвота, приступообразные боли в животе, иногда жидкий стул. Затем развивается метеоризм, что означает парез желудочно-кишечного тракта. Наиболее типичными симптомами ботулизма являются расстройство зрения (затуманенность, двоение, расширенные зрачки), затрудненное глотание, расстройство речи, мышечная слабость, параличи поперечнополосатой и гладкой мускулатуры. Летальность составляет около 40–60 %.
Clostridium botulinum представляет собой крупные спорообразующие палочки с закругленными концами размером (0,6–1,0) × (4–9) мкм, грамположительные, подвижные (перитрихи), не образующие капсул. Овальные споры располагаются субтерминально, что придает микробу вид теннисной ракетки. Строгий анаэроб. На плотных средах растет в виде небольших прозрачных колоний с ровными или изрезанными краями. На сахарно-кровяном агаре Цейслера вокруг колоний палочки ботулизма образуются зоны гемолиза. Оптимальная температура роста составляет 30–40°С, оптимальное значение pH — 7,2–7,4. Возбудитель ботулизма содержит общий О-соматический антиген и Н-антигены, по которым их делят на шесть типов: А, В, С, D, Е, F. Наибольшее значение в патологии имеют типы А, В, F.
Clostridium botulinum продуцирует два основных типа токсинов – нейротоксин и гемолизин. Нейротоксин считается одним из самых сильных из всех известных в мире биологических ядов. Смертельная доза для человека – 0,3 мкг. Споры С. botulinum высоко терморезистентны, выдерживают нагревание до 100°С в течение 3–5 ч. Токсин возбудителя ботулизма – простой белок, состоящий только из аминокислот. Токсин довольно термоустойчив и разрушается в пищевом продукте при нагревании до 80°С в течение 30 мин, а при 100°С – в течение 15 мин. Возбудитель ботулизма широко распространен в природе и часто обнаруживается в почве, навозе, на корнеплодах, в кишечнике теплокровных животных и рыб, в иле водоемов. Продукты, содержащие С. botulinum, могут иметь запах прогорклого масла, «щиплющий» вкус», рыхлую консистенцию. Однако все эти признаки непостоянны, и пищевые продукты, содержащие большую концентрацию экзотоксина, по органолептическим показателям могут не отличаться от доброкачественных. В продуктах питания, контаминированных С. botulinum, токсин иногда располагается гнездно, поэтому отравление возникает не у всех людей, употреблявших одну и ту же пищу. Причиной отравления могут быть баночные мясные, овощные, рыбные консервы, сырокопченые и соленые окорока, соленая рыба, консервированные грибы, мясо кур и уток и др. Наиболее опасными являются консервированные домашние продукты, так как в этом случае невозможно добиться полного уничтожения спор возбудителя. В большей степени это касается грибов, что связано с трудностью их отмывания от частиц земли, содержащей споры.
Для предупреждения возникновения ботулизма на пищевых предприятиях необходимо строго соблюдать санитарно-гигиенические правила. Большое значение в профилактике ботулизма имеет правильная организация технологии обработки продуктов питания, особенно при изготовлении консервов. При этом наиболее важным моментом является контроль соблюдения режимов стерилизации. Засаливать рыбу следует в крепком солевом растворе (тузлуке) с концентрацией хлорида натрия не ниже 10%. Возбудитель ботулизма чувствителен к кислой реакции среды, поэтому добавление кислот при мариновании или их накопление при квашении подавляет его размножение.
Микотоксикозы (от греч. mecos – гриб + токсикоз) – пищевые отравления, обусловленные попаданием в организм микотоксинов, образующихся в процессе жизнедеятельности ряда мицелиальных грибов. Исследователи выделили около 300 микотоксинов, продуцируемых 350 видами мицелиальных грибов. Практическое значение как контаминанты пищевых продуктов имеют около 20 из них. Наиболее распространены и опасны для здоровья человека афлатоксины В1, В2, Gl, G2, Ml, продуцируемые грибом вида Aspergillus flavus.
Так как грибами контаминированы в основном растения, микотоксины чаще обнаруживаются в растительных продуктах. Особое внимание следует обращать на обнаружение микотоксинов в продуктах животного происхождения, куда они могут попадать вследствие скармливания сельскохозяйственным животным и птице кормов, пораженных мицелиальными грибами. Такие продукты представляют наибольшую опасность для здоровья человека, так как микотоксины присутствуют в них без видимого роста плесени.
Патулин, продуцируемый грибами Penicillium patulum, Penicillium expansum, – второй из наиболее часто встречающихся микотоксинов. Он часто обнаруживается в заплесневелых яблоках, облепихе, фруктах, ягодах, овощах. Патулин обладает высокими мутагенными и канцерогенными свойствами. Он подавляет биосинтез важных для организма веществ, которые содержат группу SH.
Наиболее широко распространенными являются микотоксины трихотецены, продуцируемые грибами родов Trichothecium, Stachibotris, Trichoderma, Fusarium (Fusarium sporotrichiella, Fusarium solani, Fusarium graminearum). В этой группе насчитывается около 80 микотоксинов. Их делят на четыре типа: А, В, С и D. Представителем микотоксинов типа А является токсин Т-2; типа В – дезоксиниваленон (ДОН); типа С – роридин; типа D – кротоцин.
Одним из наиболее токсичных трихотеценовых микотоксинов является токсин Т-2. Он ингибирует синтез белков в эукариотической клетке и таким образом оказывает патогенное воздействие на организмы животных и людей, которое проявляется в виде анемии и иммунодепрессии, кровотечения, рвоты, некрозов слизистых оболочек и дерматитов. Токсин Т-2 действует на кроветворные органы, центральную нервную систему, вызывает лейкопению, геморрагический синдром,
Группа зеараленона и его производных включает 15 микотоксинов. Продуцентом зеараленона является гриб Fusarium graminearum. Fusarium graminearum часто обнаруживается в кукурузе, иногда в пшенице, ячмене, овсе, сорго, а также в масле и крахмале, полученном из кукурузы, содержащей зеараленон, который вызывает общее отравление организма.
Охратоксин продуцируется грибом Aspergillus ochraceus и содержит три химически родственных токсических метаболита – охратоксины А, В и С. Охратоксин А продуцируется преимущественно грибом А. ochraceus, а также грибами рода Penicillium: P. viridicatum, P. variabile, P. cyclopium. Охратоксины подавляют метаболизм у животных в части синтеза белковых веществ, нарушают обмен гликогена.
Фумонизины продуцируются грибами Fusarium moniliform и Fusarium proliferatum, обладающими канцерогенным действием и вызывающими цирроз печени.
Содержание микотоксинов: афлатоксина В, дезоксиниваленона, зеараленона, токсина Т-2, патулина, фумонизина регламентируется в продовольственном сырье и пищевых продуктах растительного происхождения; афлатоксина M – в молоке и молочных продуктах. В пищевых продуктах предельная допустимая доза афлатоксина В составляет 0,005; патулина – 0,05; токсина Т-2 – 0,1; дезоксиниваленона – от 0,5 до 1,0 – в зависимости от сырья и пищевого продукта; зеараленона – 1,0; фумонизина – 0,2 мг/кг.
Эрготизм. Заболевание человека и животных под названием эрготизм возникает в результате скармливания и употребления в пищу злаков, пораженных спорыньей (Claviceps purpurea). Токсичной является покоящаяся стадия гриба – «рожки спорыньи» фиолетового цвета. В рожках содержатся алкалоиды лизергиновой кислоты и клавиновые производные. Эти токсические вещества устойчивы к нагреванию и сохраняют токсичность после термической обработки. Длительное хранение зерна не инактивирует токсины спорыньи. Отравление проявляется в виде судорог, конвульсий, поражения центральной нервной системы, острого гастроэнтерита, некрозов периферических частей тела. В тяжелых случаях наблюдаются галлюцинации, расстройство сознания, эпилептические судороги (отсюда название «злая корча»). Отравление может закончиться летальным исходом. При выздоровлении наблюдаются парезы, атрофия мускулатуры.
Контрольные вопросы и задания
- Назовите группы микроорганизмов – индикаторов микробиологической безопасности пищевых продуктов.
- Дайте общую характеристику санитарно-показательных микроорганизмов (СПМО) и укажите требования к ним.
- Опишите группы СПМО: мезофильные аэробные и факультативно анаэробные микроорганизмы (КМАФАнМ); бактерии группы кишечной палочки (БГКП – колиформные бактерии); энтерококки; кишечные бактериофаги.
- Охарактеризуйте условно-патогенные микроорганизмы: Escherichia coli, Staphylococcus aureus, Bacillus cereus, сульфитредуцирующие бактерии (Clostridium perfringens), бактерии рода Proteus, Vibrio parahaemolyticus и другие микроорганизмы (Enterobacter sakazakii, бифидобактерии, бактерии рода Yersinia, бактерии рода Campylobacter).
- Опишите патогенные СПМО: сальмонеллы, Listeria monocytogenes.
- Охарактеризуйте возбудителей антропонозных заболеваний, передающихся пищевым путем: холеры, дизентерии, брюшного тифа и паратифов А и В.
- Дайте определение и назовите причины пищевых токсикоинфекций.
- Каковы основные характеристики эндотоксинов бактерий?
- Перечислите особенности сальмонеллы как возбудителя токсикоинфекций.
- Охарактеризуйте возбудителей пищевых интоксикаций (токсикозов): стафилококков, стрептококков, возбудителя ботулизма.

